|
第 21 卷第 8 期 疫情報導 605 常用市售流感快速檢測試劑之效能比較
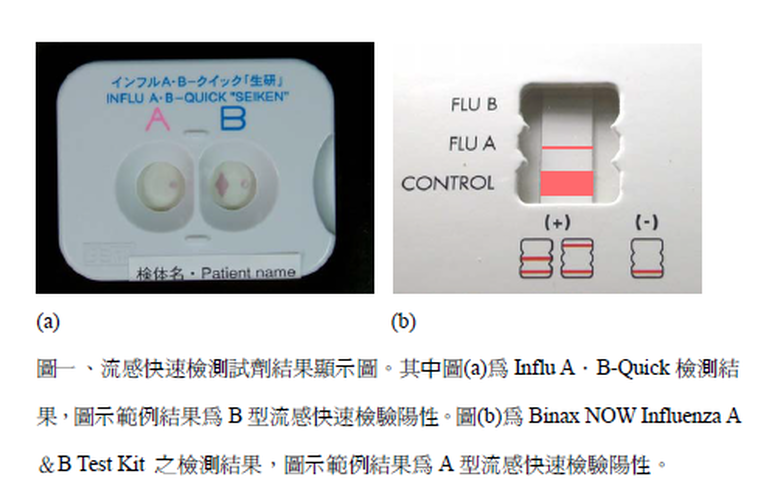
*邱淑君、林智暉、林永政、李政壕、陳豪勇 行政院衛生署疾病管制局研究檢驗中心 摘要 流感病毒為每年冬季最活躍的呼吸道病原之一,由於具有高度傳染性,容易在社區間造成群聚性的感染,為快速鑑定流感病毒,本試驗針對市售三種流感病毒快速檢測試劑Influ A.B-Quick、BinaxNow Influenza A&B Test kit以及QuickVue Influenza A+B test進行專一性及靈敏度之評估,並與Real time RT-PCR及病毒培養等檢測方法進行比較。測試結果三種快速檢測試劑其靈敏度分別為30%、70%以及90%,而專一性則均可達90%以上,顯示目前市售流感快速檢測試劑可正確且快速檢測檢體中病毒含量較高之流感病毒陽性檢體,可提供作為緊急檢體及疑似流感群聚感染之初步鑑定,以利防治工作之進行。本次測試之三種市售快速檢測試劑均可檢出H5N1型之A型流感病毒,目前國內雖無疑似人感染禽流感的案例發生,但此快速檢測試劑應可備於機場海關,當發現入境旅客具有發燒症狀時,可透過快速檢測試劑進行初步檢測,以防止新型流感趁隙入侵。 前言 流感病毒具有高度傳染性,感染年齡層遍及所有族群,而對年長者特別具有高致死率(3,7)。流感病毒的標準檢驗方法為病毒分離(virus isolation),也就是藉由細胞培養的技術分離病原體。然而細胞培養需花費7-10天的時間,操作的過程也需要無菌的操作環境以避免環境因素影響細胞及病毒的生長,因此目前研發出許多市售流感病毒快速檢測系統,將流感病毒偵測的時間縮短至幾個小時,可在流感病毒偵測初期,便能加以確認並且快速啟動防疫機制,例如投藥或者是隔離等,以達到快速防疫的目的(4,5)。 目前最常被應用的快速檢驗方法有兩種,一種為應用real time PCR的分生技術,將病毒核酸純化出來後,利用PCR方法將偵測片段加以放大,之後利用專一性的探針(Probe),將訊號以螢光方式呈現機器讀取後便能判定採檢檢體內是否有流感病毒存在。而此項real time RT-PCR更能利用multiplex技術藉由螢光波長的不同,將流感病毒進行次分型(1)。而另一種快速檢驗方法則為偵測流感病毒的核蛋白(necleoprotein),統稱快速檢測試劑(rapid test),利用酵素免疫原理(enzyme-linked immunosorbent assay)可初步檢測檢體中是否有A型或 B型流感病毒。這種快速檢測試劑因能快速進行確認最常被應用於疑似呼吸道病毒感染之群聚事件(3,4),而國內應用最具成效的經驗便是在國內爆發SARS疫情期間,由於流感以及SARS在發病的初期症狀非常相近,必須快速鑑別區分檢體,利用快速檢測試劑可以快速區分流感及SARS病毒,以降低民眾恐慌以及協助臨床醫師研判及治療上的困難。 目前市面上有許多市售的流感快速檢測試劑,絕大部分均能在30分鐘以內操作完成並進行判讀,由於各種產品在靈敏度(sensitivity)以及專一性(specificity)均有所差異(3-5),本文謹從市售的試劑中,挑選三種目前在國內被廣泛使用的試劑組,包括Influ A.B-Quick(Denka Seiken)、QuickVue Influenza A+B test (Quidel, SanDiego, Calif)、BinaxNow Influenza A&B Test kit(Binax)以及進行評估,並同時與另一種快速檢驗方法real time RT-PCR以及細胞培養法,以臨床檢體進行平行測試。 材料與方法 檢體 患者產生下列部份或全部症狀,包括高燒超過38.5℃、咳嗽、喉嚨痛、頭痛、肌肉酸痛及流鼻水等時,在發病日起三到五日內以病毒性咽喉拭子(Copan company)採取上呼吸道檢體,並以病毒運送培養基將檢體以低溫(4℃-8℃)保存,並在採檢後三日內送至本局昆陽研究檢驗中心呼吸道病毒檢驗室,進行病毒培養、分離與鑑定。 病毒培養 將咽喉拭子與1mL運送培養液充分攪拌,使病毒自棉棒脫離至培養液中,將培養液取出,取100μL檢體接種至培養管(culture tubes)內的Madin-Darby canine kidney (MDCK)細胞,然後加入不含胎牛血清的DMEM培養液、TPCK(tosylsulfonyl phenylalanyl chloromethyl ketone)treated trypsin (Sigma, St. Louis, Mo.)、及抗生素。每天觀察細胞是否有細胞病變(cytopathic effect, CPE),觀察期為14天,若細胞出現CPE,則立即離心收取上清液,沉澱下來的細胞碎片以1 mL PBS洗下存於4℃冰箱。所有檢體當觀察期結束後,亦經離心收取上清液,之後沉澱物加入1mL PBS溶液,將細胞由培養管上刮下,固定於玻片上進行免疫螢光染色。MDCK細胞之繼代培養過程均使用各種不同濃度之標準病毒液及陰性對照組進行感染細胞培養,以檢查比對MDCK細胞的敏感度是否有異。 免疫螢光染色法 將接種檢體之細胞培養管以3000 rpm離心15分鐘收取上清液,並將離心沉澱之疑似感染細胞以利用市售螢光檢測試劑(CHEMICON International, Inc)以間接免疫螢光染色法(indirect immunofluorescence assay,IFA),染色後,以螢光顯微鏡進行鏡檢,細胞質出現蘋果綠(apple green)螢光則判定為流感病毒陽性。 Influ A.B-Quick Influ A.B-Quick試劑組是由日本SEIKEN廠商所研發的一種流感快速檢驗試劑套組,其檢測原理是利用酵素免疫法(EIA),使用流感病毒共同核蛋白的特異性單株抗體,以快速檢測咽喉、鼻咽拭子、及鼻腔抽取液中的A型或B型流感病毒。操作過程是依循製造廠商的檢驗操作步驟來進行,將檢體採樣棉棒浸入套組所提供之檢體緩衝溶液中,以vortex混合均勻後將棉棒取出,檢體以內附的濾膜蓋過濾,未經過濾的檢體可能會導致偽陽性的結果。整個試驗均在室溫的環境中操作,將已經過濾的檢體,分別滴入已標記A與B檢測孔之檢測盤中,等檢體完全滲入檢測孔後,再滴入5滴試劑組提供之A型及B型抗體進行酵素連結反應。待試劑完全滲入檢測孔後,再滴入5滴試劑組所附之清洗液進行wash步驟,之後加入5滴呈色液進行呈色步驟,整個過程於15分鐘內即可完成,檢驗結果的目測判讀在終止劑加入後約5分鐘時進行,檢測盤的A與B檢測孔中,都應出現紫紅色呈色圓點,才算是有效的檢驗,如未出現呈色點,則將結果列為無法判讀(indeterminate)。 QuickVue Influenza A+B Test QuickVue Influenza A+B test試劑是由美國QUIDEL廠商所研發的一種流感快速檢驗試劑套組,其檢測原理是利用對流感病毒nucleoprotein (NP) 具專一性之單株抗體,以快速偵測咽喉、鼻咽拭子、及鼻腔抽取液中的A型或B型流感病毒。操作過程是依循製造廠商的檢驗操作步驟來進行。將試劑組所附之溶液(reagent)滴入測試玻璃管中,搖晃玻璃管使管內粉末徹底溶解,檢體採樣棉棒與運送培養基經vortex混合均勻後將棉棒取出混合均勻,取200μL加入測試玻璃管中,並與反應溶液混合均勻。之後將反應檢測條(strip)放入反應玻璃管中,使溶液隨反應條吸附而上,整個試驗均在室溫的環境中操作,置放10分鐘後將檢測條取出,並判讀反應檢測條上的結果。 Binax NOW Influenza A&B Test Kit Binax NOW Influenza A&B Test Kit試劑是由美國Binax廠商所研發的流感快速檢驗試劑套組,其檢測原理也是利用流感病毒核蛋白抗原(nucleoprotein antigens)具專一性單株抗體偵測所採檢體中之A型或B型流感病毒。操作過程是依循製造廠商的檢驗操作步驟來進行。檢體採樣棉棒與運送培養基經vortex混合均勻後將棉棒取出。將以鋁箔包裝之測試反應組取出,取100μL病毒液加入測試玻反應條上方區塊使檢體吸附。待檢體完全被吸附後,撕去測試組右方棕色膠帶,密封檢測試劑。整個試驗均在室溫的環境中操作,置放15分鐘後由觀察視窗進行結果之判讀。 Real time RT-PCR 以QIAGEN 的QIAamp Viral RNA Mini Kit (Cat. No. 52906)進行RNA的萃取,操作步驟均依據試劑組所附之標準操作程序進行。於560 μL Buffer AVL中加入140 μL 的檢體於室溫下作用10分鐘,再加入560μL高純度酒精混合完全(vortexing),將混合液通過QIAamp spin column,column 以緩衝液AW1 及AW2清洗,再以純水 (RNase free water) 將RNA溶出,立即進行Real time RT-PCR反應,或置於-20℃中儲存備用。 試驗所使用的核酸引子對(primer)以及核酸探針(probe)序列參考並選擇已經發表的研究(6,8) 其中,Influenza A的核酸探針標記的dye為Fam,Influenza B的核酸探針標記的則為Vic。Real time RT-PCR實驗以ABI廠牌之TaqMan One-step RT-PCR Master Mix Reagents (Part Number:4309169) 進行試驗,反應總體積為25μL,取5 μL前步驟萃取之RNA作為反應模板(template),各個引子濃度為0.4 μM,各核酸探針濃度為0.1 μM。real time PCR試驗的反應條件為:(1)RT:40℃,30分鐘。(2)Denature:95℃,10分鐘。(3)Amplification:95℃,15秒;60℃,1分鐘。待儀器完成偵測後,使用儀器之自動分析程式進行檢驗結果之分析及Ct值之判讀。將偵測視窗切換至設定之Flu A時,可見到A型流感陽性檢體螢光上升曲線;若將檢測視窗切換至設定之FluB,若有陽性檢體,則可在視窗內見到該檢體之螢光上升曲線,目前此對設計之primer 及probe 之靈敏度,經由將標的基因片段以pEGM-T easy試劑組(Invitrogen Corporation)選殖至載體(pEGM-T)中,作為標準樣品(standard) 。將已定量之標準DNA做10倍序列稀釋(10 X serial dilution)後,進行即時反轉錄PCR試驗以建立標準曲線,如圖二所示,本偵測系統之靈敏度可達檢測體積25 μL內僅含 1個copy之病毒量。 結果 由於本次試驗目的之一是初步比較瞭解各市售試劑對臨床檢體檢驗敏感度之差異,故依據定醫診所之採檢情形,各試劑組均僅以一組為此次測試之樣本。以本局定醫診所就診之26位患者,利用病毒性拭子採集其咽喉部位檢體後進行檢測,其中患者的年齡層分佈主要以學齡兒童為主,年齡平均為9.71歲。最年長的為35.5歲,年齡最小者為3.2歲。性別比例方面為男生有14位,女生為12位,比例約為1:1。26支臨床檢體中經由細胞培養為流感病毒陽性共10支,其中6支為A型流感病毒,4支為B型流感病毒。而其他16支臨床檢體的病毒培養結果包括流感病毒、腺病毒、副流感病毒以及呼吸道融合病毒、單純疱疹病毒細胞培養結果均為陰性,並未分離出任何病毒。經由血球凝集抑制法(HI test)進行流感病毒血清型別分析,6支分離出之A型流感均為A/H3次型別,而4支B型流感病毒則屬於B/Yamagata族群。 檢體經三種快速檢驗試劑之檢驗情形,26支檢體中檢出A型流感支數,QuickVue試劑為7支,Binax試劑6支,Influ A.B-Quick為3支。而B型流感的檢出情形依前順序分別為2支、1支,而Influ A.B-Quick則未檢出B型流感。以病毒培養陽性為真實陽性作為標準對照,比較各試劑組之靈敏度及專一性,如表一所示,發現在靈敏度方面以QuickVue為最佳,達90%。而專一性的比較上除QuickVue為93.8%,其他兩組均為100%。此外,經由real time RT-PCR檢測,共有8支為A型流感陽性,4支為B型陽性。而所有培養出來的流感病毒陽性檢體,均包含於real time RT-PCR的陽性檢體之中。 討論 三種快速檢測試劑在操作及檢測方法的比較上,如表二所示,三種試劑均可同時檢測A型及B型流感病毒,在操作過程中,因Influ A.B-Quick須 操作的試劑數較多,反應窗吸附檢體所需時間也較久,需要花費較多時間。而且由於須透過圓形視窗進行判讀,因判讀視窗具些許高度,弱陽性之檢體容易因反應膜反光而影響判讀(圖一a)。此外Influ A.B-Quick臨床檢體須經試劑組所附之過濾膜過濾,或許會因部分病毒粒子被濾膜隨雜質被擋於濾膜之前而降低檢測效果,靈敏度僅30%。 Binax Now Influenza A&B Test Kit在操作上與QuickVue相同,均以試劑組所含之檢測條吸附原臨床檢體後,以反應結果線出現的有無進行判讀。但因Binax Now Influenza A&B Test Kit陽性判讀之反應結果線較細,若為弱陽性檢體便可能因反應線不明顯或判讀經驗不足而被忽略(如圖一b)。 QuickVue在三者中靈敏度高且判讀容易,而此次試驗所檢出之七支A型流感病毒中,有一支其病毒培養結果為陰性。此件檢體經real time RT-PCR檢測,亦為A型流感PCR檢驗陽性,Ct值為27.09。故推測可能此件檢體雖然疑似帶有A型流感病毒,但可能因為採檢後保存不當,亦或是送回實驗室檢驗的運送過程中因有失誤而導致病毒喪失活性,無法培養成功。QuickVue的靈敏度高,操作容易且所需花費時間最短,為本試驗三組中效果最好,此項檢驗結果與前人研究相符合(4,13),但因價格相較於其他兩組為高,使用者在使用上須考慮其成本。 流感病毒快速檢驗試劑組在操作方法上相當的簡單及方便,在半小時之內便可獲得初步檢驗結果,而且不一定需要由專業技術人員才能操作。且在面對疑似流感群聚感染事件時,做為防疫上重要的參考依據(12)。目前國內面對流感病毒感染患者,所使用的抗流感藥物以克流感(Tamiflu)為主,然若經由流感快速試劑檢驗確認流感病毒型別(A型或B型),臨床醫師便可依據病毒型別的不同來選擇較為便宜的 Amantadine 或 Rimantadine 但是只對A型流感有效,或是對於A型及B型流感均有效的神經胺酸酶抑制劑 (例如 Zanamivir )等,可提供臨床醫師用藥參考(2)。 目前國外發表文獻中並無將此三種快速檢測試劑進行靈敏度及專一性比較之報告,尤其是BinaxNow Influenza A&B Test kit則未查有相關文獻探討。而本次測試選擇此三種快速檢測試劑包括Influ A.B-Quick、BinaxNow Influenza A&B Test kit以及QuickVue Influenza A+B test進行比較之原因,在於此三種快速檢測試劑均為本局自SARS疫情以來爲能讓實驗室及臨床醫師可快速區分流感及SARS病毒,同時也應用在機場進行發燒旅客初步檢驗使用,進而推廣給全省衛生局所、機場以及本局病毒性合約實驗室所使用之流感快速檢測試劑套組。進行相關評估後之初步資料,可作為未來進行流感大流行防治計畫時選擇試劑之參考依據。 RRT-PCR檢驗法為目前最被應用於緊急檢體之檢測技術(9-11),也是當下偵測新型流感進入國內與否的最佳利器,利用核酸引子及專一性探針之實驗設計,經由儀器進行判讀後便可由電腦圖檔對檢驗結果進行研判,透過標準曲線之訂定便可將檢體所含病毒加以定量(圖二)。不但具有高敏感度及特異性的優點,且可在檢體經RNA進行核酸純化後,1-3小時內便可有初步的檢驗結果,並可同時進行次型別鑑定 (6,9,14)。而本次實驗結果同時顯示RRT-PCR檢驗法為所有檢測法中靈敏度為最高,若以本次總檢體數26 支而言,病毒培養共10支陽性,陽性率為38.5%,而 RRT-PCR測得陽性檢體共12支,陽性率46.1%。曾有學者建議是否該變更定義PCR陽性即可確認為真實陽性個案,但最後定論仍有待專家學者們達成共識(3,10,11)。 目前國際禽流感疫情風雨飄搖,隨時都有入侵國內的可能,本次檢驗最大的收穫,便是目前經檢測的快速檢驗試劑,均能偵測禽流感病毒,倘若有疑似新型流感病毒個案發生,可利用市售流感快速檢驗試劑初步加以釐清,若檢驗出為A型流感,也可藉由RRT-PCR技術在數小時內快速加以確認。目前本局研究檢驗中心均已針對新型流感之偵測,建立整套的檢驗流程及相關檢驗技術,因其操作上需更高專業的技術及複雜的機器設備,檢驗操作人員在平日便須接受良好的訓練,並維持相當的檢驗技術水平,以能隨時應付突發狀況。 參考文獻 1. 邱淑君、林智暉、賴淑寬等。流感與SARS病毒分子生物學快速檢驗方法之研究開發。疫情報導,第二十卷第三期:197頁-205頁。 2. 林智暉、邱淑君、張佳琪等。預防與治療流行性感冒的新選擇。疫情報導第十六卷第十一期:525頁-530頁。 3. Barker, WH., and Mullooly, JP. Pneumonia and influenza death during epidemics, implication for prevention. Arch. Intern. Med. 1982; 142:85-89. 4. Ruest, A., Michaud, S., Deslandes, S., et al: Comparison of the Directigen Flu A+B Test, the QuickVue Influenza Test, and Clinical Case Definition of Viral Culture and Reverse Transcription-PCR for Rapid Diagnosis of Influenza Virus Infection. J Clin Microbiol 2003; 41:3487-3493. 5. Cazacu, AC., Chung SE., Greer J, et al: Comparison of the Directigen Flu A+B Membrane Enzyme Immunoassay with viral Culture for Rapid Detection of Influenza A and B Viruses in Respiratory Specimens. J Clin Microbiol 2004; 42: 3707-3710. 6. van Elden LJ, Nijhuis M, Schipper P, et al: Simultaneous detection of influenza viruses A and B using real-time quantitative PCR. J Clin Microbiol 2001; 39:196-200. 7. Sakuma T. Infant Influenza. Acta Pediatrica Japonica. 1997; 39:669-675. 8. Wright KE, Wilson GAR, Novosad D, et al: Typing and subtyping of influenza viruses in clinical samples by PCR. J Clin Microbiol 1995; 33:1180-1184 9. Zou S. A practical approach to genetic screening for influenza virus variants. J 10. Barenfanger J, Drake C, Leon N, et al: Clinical and financial benefits of rapid detection of respiratory viruses: an outcomes study. J Clin. Microbiol. 2000; 38: 2824-2828 11. Herrmann B, Larsson C, and Zweygberg BW. Simultaneous detection and typing of influenza viruses A and B by a nested reverse transcription-PCR: comparison to virus isolation and antigen detection by immunofluorescence and optical immunoassay (FLU OIA). J. Clin. Microbiol. 2001; 39:134-138 12. Zambon, M., J. Hays, A. Webster, et al: Diagnosis of influenza in the community: relationship of clinical diagnosis to confirmed virological, serologic, or molecular detection of influenza. Arch. Intern. Med. 2001; 161:2116-2122. 13. Pregliasco F, Puzelli S, Mensi C, et al: Influenza virological surveillance in children: The use of the Quickvue rapid diagnostic test. J Med Virol. 2004; 73:269-73. 14. Stone, B., Burrows, J., Schepetiuk. S. et al: Rapid detection and simultaneous subtype differentiation of influenza A viruses by real time PCR. J Virol Methods. 2004; 117:103-12.
0 評論
發表回覆。 |
类别
全部
Find all the info that you need about " billig munnbind hardworkout " at https://hardworkout.no
|
|
|
|
關於本站 |
關於站長謝謝查詢,稍後補充 !
|
聯絡我們 |
|
站長區 |
Copyright © 2013 醫訊站 Clinic24HK.Com. 版權所有 (欄位「醫療組織介紹」及其他連結版面資料除外) 歡迎轉載 (唯必須註明「資料引自 - 醫訊站: http://www.clinic24hk.com」+ 按此留言告知,敬請備悉,謝謝合作 ! )